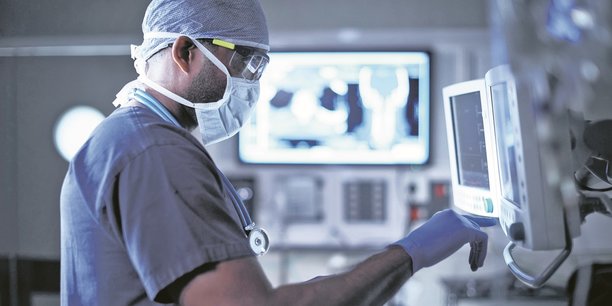
« Si nous avons choisi Paris, c'est parce que je suis français, déclare en plaisantant Serge Bernasconi, le PDG de MedTech Europe, l'association des professionnels du secteur du dispositif médical et du diagnostic. Plus sérieusement, si l'équivalent du Snitem au niveau européen a décidé, pour la première fois, de quitter Bruxelles, où il tenait chaque année son évènement depuis dix ans pour s'inscrire dans le sillage de la Journée start-up innovantes du Snitem, c'est avant tout parce que les professionnels européens veulent saluer le dynamisme du secteur dans l'Hexagone. « Dans le domaine du dispositif médical et du diagnostic, la France est l'un des pays européens qui produit le plus d'innovations, depuis de nombreuses années », relève ainsi Serge Bernasconi. D'ailleurs, MedTech Europe participe tous les ans à la journée organisée par le Snitem. Quoi de plus naturel, dans ces conditions, que de s'en rapprocher un peu plus ? « Nous espérons ainsi que les start-up présentes à la journée du Snitem pourront aussi tirer des enseignements de notre forum », poursuit le PDG de l'association européenne. Le MedTech Forum se tiendra les 15 et 16 mai, dans la foulée de la Journée start-up innovantes, à la Cité des sciences et de l'industrie.
Désormais, en effet, toute aventure entrepreneuriale et commerciale prenant sa source dans une innovation technique et médicale ne peut se concevoir qu'en visant le marché européen, voire mondial. En outre, MedTech Europe veut attirer l'attention des professionnels français sur l'évolution de la réglementation européenne.
Parcours réglementaire
Une évolution très impactante, et qui sera au coeur des débats menés à l'occasion du forum. Pour suivre les innovations, nombreuses, l'Europe a en effet décidé, il y a quelque temps, de revisiter ses règles de mise sur le marché des dispositifs médicaux et de diagnostic. Sous-tendue par un souci de sécurité et une exigence d'efficacité accrus des dispositifs et diagnostics pour les patients, la réglementation sera plus contraignante. Pour les sociétés qui voudront obtenir le la certification européenne (marquage CE medical), cela signifie, selon MedTech Europe, un nouveau parcours, complexe, long et délicat. Et pour cause, la nouvelle réglementation est passée d'une vingtaine d'articles à plus de 120 ! Elle entrera en vigueur en mai 2020 pour les dispositifs médicaux et en mai 2022 pour les diagnostics in vitro. « La transition sera ardue, compte tenu du fait que le système s'appuie sur la décentralisation, grâce à des organismes publics, ou privés mais contrôlés par les Etats, et qui certifieront les dispositifs médicaux et de diagnostic pour toute l'Europe », explique Serge Bernasconi. Alors qu'il existe actuellement pas moins de 500 000 dispositifs médicaux en Europe, dont la certification doit être, qui plus est, renouvelée tous les cinq ans, la stratégie d'avoir une cinquantaine d'organismes à travers l'Europe, certifiant les entreprises pour la mise sur le marché de l'Union est hasardeuse, selon MedTech Europe. « Et s'il n'y en a qu'une douzaine dans un premier temps, selon l'engagement de la Commission européenne, ce ne sera pas assez, poursuit-il, en notant que pour l'instant, il n'en existe qu'un seul - et il est au Royaume Uni... « Imaginez qu'il y ait un hard Brexit ! », ajoute-il. L'organisme britannique serait inopérant pour le reste de l'Europe...
Pour l'heure, le parcours de certification d'un dispositif médical ou de diagnostic prend déjà entre trois et neuf mois. Face à la nouvelle complexité de l'exercice, associée à la pénurie d'organismes certificateurs en Europe, « on imagine mal comment 50 000 à 100 000 dispositifs seront certifiés ou re-certifiés tous les ans », poursuit le dirigeant de l'association professionnelle européenne. A moins que certains organismes nationaux ne le fassent de manière indépendante, mais dans ce cas, quid de l'harmonisation européenne ? Et quid de l'égalité des patients devant l'accès aux dispositifs médicaux et de diagnostic dont ils ont besoin ?
En pleine période électorale européenne, une telle incertitude aurait de quoi susciter la défiance des citoyens vis-à-vis des instances européennes... A n'en pas douter, les débats sur la nouvelle réglementation seront animés, au MedTech Forum, qui attend environ 1000 participants. Mais si l'organisation professionnelle tire d'ores et déjà la sonnette d'alarme, c'est pour mieux sensibiliser les acteurs du secteur sur les enjeux - sans oublier la Commission européenne...
Le Forum sera également l'occasion de débattre d'autres thèmes, tels que la santé et le numérique, l'accès au marché et les politiques économiques, ainsi que les questions juridiques, de compliance et d'éthique pour l'industrie.


 « Quand nous mettrons le pied sur l'accélérateur, nous serons difficiles à égaler » (Joelle Pineau, directrice de la recherche en IA chez Meta)
« Quand nous mettrons le pied sur l'accélérateur, nous serons difficiles à égaler » (Joelle Pineau, directrice de la recherche en IA chez Meta)

Il n'y a actuellement aucun commentaire concernant cet article.
Soyez le premier à donner votre avis !