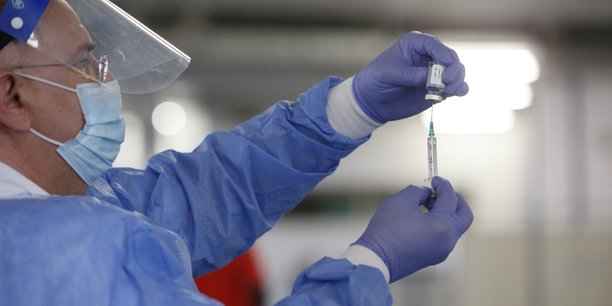
L'Agence européenne des médicaments (EMA) a estimé mercredi que les caillots sanguins devraient être répertoriés comme effet secondaire "très rare" du vaccin AstraZeneca contre le Covid-19.
L'EMA a établi "un lien possible avec de très rares cas de caillots sanguins inhabituels avec des plaquettes sanguines basses", a déclaré l'agence basée à Amsterdam dans un communiqué, indiquant toutefois que la balance bénéfice/risque reste "positive". Fin mars, l'autorité avait déjà rendu un avis selon lequel le vaccin est "sûr et efficace" et n'est pas lié à un risque plus élevé de caillots sanguin.
Pour rappel, à la fin juin, la France devrait avoir reçu plus de 15 millions de doses d'AstraZeneca sur un total de 72 millions livraisons, selon les prévisions de la Direction Générale de la Santé au 23 mars. Il est le deuxième type de vaccin le plus administré dans l'Hexagone, après l'Américain Pfizer.
Au Royaume-Uni, où le vaccin a été conçu avec les chercheurs de la Oxford University, le régulateur britannique a fait état mardi de 19 morts sur 79 signalements de caillots sanguins. Il assure lui aussi que les bénéfices restaient supérieurs aux risques pour "la grande majorité" de la population.
Mais dans le même temps, le comité scientifique supervisant la campagne de vaccination anti-Covid au Royaume-Uni a recommandé de limiter l'usage du AstraZeneca aux plus de 30 ans quand c'est possible, après le signalements de rares cas de caillots sanguins.
"Les adultes âgés de 18 à 29 ans, qui n'ont pas de comorbidité leur faisant encourir un risque plus élevé d'une forme grave de la maladie Covid-19, devraient se voir proposer un autre vaccin Covid-19 plutôt que le vaccin AstraZeneca, quand une telle alternative est disponible", a déclaré le professeur Wei Shen Lim, du JCVI, soulignant que le comité ne recommandait l'arrêt de la vaccination dans aucun groupe d'âge.
> Dossier - la course aux vaccins
De son côté, l'EMA n'a pas identifié de facteur de risque spécifique concernant le vaccin, estimant qu'une explication "plausible" à des cas rares de caillots sanguins pourrait être une réponse immunitaire.
"Des facteurs de risque spécifiques tels que l'âge, le sexe ou les antécédents médicaux n'ont pas pu être confirmés car les événements rares sont observés à tous les âges", a déclaré la directrice exécutive de l'EMA, Emer Cooke, lors d'une visioconférence.
Une polémique qui ne s'éteint pas
Après plusieurs suspensions temporaires du vaccin - y compris en France -, le sérum avait finalement été autorisés. Mais mercredi, la région espagnole de Castille-et-Léon (nord-ouest) a annoncé suspendre AstraZeneca dans l'attente de la publication du rapport de l'Agence européenne des médicaments. Sa conclusion devrait donc lever la suspension.
La veille, l'université d'Oxford a annoncé qu'elle suspendait les essais sur les enfants du vaccin qu'elle a développé avec le laboratoire anglo-suédois, dans l'attente de l'avis du régulateur britannique. "S'il n'y a pas d'inquiétude concernant la sécurité de l'essai clinique pédiatrique, nos attendons des informations complémentaires du MHRA", le régulateur britannique, "sur les cas rares de thromboses qui ont été rapportés chez des adultes, avant de procéder à de nouvelles vaccinations dans l'essai", a indiqué l'université britannique dans un communiqué.
En France, la famille d'un homme de 63 ans, décédé en mars en Haute-Savoie de "multiples thromboses" après avoir reçu une première injection du vaccin anti-Covid d'AstraZeneca, a déposé plainte contre X pour "homicide involontaire", a appris mardi l'AFP auprès du parquet d'Annecy.
Il ne s'agit pas là de la première procédure visant le vaccin du laboratoire : une plainte contre X a été déposée à Toulouse après la mort d'une femme de 38 ans et le parquet de Nantes a ouvert une enquête préliminaire à la suite du décès d'un étudiant en médecine.
(Avec AFP)